Một loại than đá có chứa 3,2% X là S 96,8% C .Tính khối lượng than đá cần dùng để tạo thành 56 lít hỗn hợp khí

Những câu hỏi liên quan
Quặng than đá có chứa 3%S và 5% tạp chất không đáy. Tính khối lượng õi cần dùng để đốt cháy 2kg than đá đó
PTHH: \(C+O_2\underrightarrow{t^o}CO_2\)
Ta có: \(m_C=2\cdot92\%=1,84\left(kg\right)\) \(\Rightarrow n_C=\dfrac{1,84}{12}=\dfrac{23}{150}\left(kmol\right)=n_{O_2}\)
\(\Rightarrow m_{O_2}=\dfrac{23}{150}\cdot32\approx4,91\left(kg\right)\)
Đúng 1
Bình luận (0)
Đề có phải thiếu: "Còn lại là Cacbon"
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 7,5g than đá (biết than đá có thành phần chính là C, chứa 4% tạp chất không cháy) thu được CO2. Thể tích O2 cần dùng (đkc) để đốt cháy hết lượng than đá trên là?
Ta có: mC = 7,5.(100 - 4)% = 7,2 (g)
\(\Rightarrow n_C=\dfrac{7,2}{12}=0,6\left(mol\right)\)
PT: \(C+O_2\underrightarrow{t^o}CO_2\)
Theo PT: \(n_{O_2}=n_C=0,6\left(mol\right)\Rightarrow V_{O_2}=0,6.24,79=14,874\left(l\right)\)
Đúng 1
Bình luận (0)
đốt một mẩu than đá (chứa hợp chất không cháy) có khối lượng 0,6 kg trong oxi dư , thu được 1,06m3 (điều kiện tiêu chuẩn) khí cacbonic . tính thành phần phần trăm khối lượng của cacbon trong mẫu than đá trên .
C + O2 => CO2
1,06m3 = 1060 (l) => nCO2 = \(\frac{1060}{22,4}=47,32mol\)
nC = nCO2 = 47,32 mol
=> mC = 47,32.12 = 567,84 (g)
m than đá = 0,6kg = 600g
=> % C = \(\frac{567,84}{600}.100\%\) = 94,64%
Đúng 0
Bình luận (0)
C + O2 CO2
1,00mol 1,00mol
47,3 mol = 47,3 (mol)
Phần trăm khối lượng của C trong mẫu than đá: = 94,6%
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 7,5 gam than đá có chứa 4% tạp chất không cháy. Thể tích khí oxi cần dùng (đktc) để đốt cháy hết lượng than đá trên là *
\(n_C=\dfrac{7,5.96\%}{12}=0,6\left(mol\right)\\ C+O_2-^{t^o}\rightarrow CO_2\\ n_{O_2}=n_C=0,6\left(mol\right)\\ \Rightarrow V_{O_2}=0,6.22,4=13,44\left(l\right)\)
Đúng 0
Bình luận (0)
Đốt một mẫu than đá (chứa tạp chất không cháy) có khối lượng 0,600kg trong oxi dư, thu được 1,06 m3 (đktc) khí cacbonic. Tính thành phần phần trăm khối lượng của cacbon trong mẫu than đá trên.
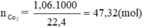
C + O2 → CO2
47,32 ← 47,32 (mol)
Theo pt: nC = nCO2 = 47,32 mol ⇒ mC = 47,32. 12 = 567,84 g
% khối lượng của C là:

Đúng 1
Bình luận (1)
Đốt một mẫu than đá nặng 0,6 gam trong không khí (dư) thu được 1,06 lít khí cacbonic . Tính thành phần phần trăm theo khối lượng cacbon trong mẫu than đá trên.
C + O2 \(\xrightarrow[]{t^o}\) CO2
nCO2 = \(\dfrac{1,06}{22,4}\approx0,047mol\)
Theo pt: nC = nCO2 = 0,047 mol
=> mC = 0,047.12 = 0,564g
%mC = \(\dfrac{0,564}{0,6}.100\%=94\%44\)
Đúng 2
Bình luận (2)
$C + O_2 \xrightarrow{t^o} CO_2$
n C = n CO2 = 1,06/22,4 = 53/1120(mol)
m C = 53/1120 .12 = 0,568(gam)
Suy ra :
%C = 0,568/0,6 .100% =94,67%
Đúng 1
Bình luận (0)
đốt cháy 10 gam than đá trong oxi dư, thu được 16,8 lít khí cacbonic(đktc) và 560ml khí sunfurơ(đktc)
a, Tính độ tinh khiết của loại than đá trên(Biết rằng trong than đá cacbon là thành phần chính)
b, Tính thể tích khí oxi ở đktc đã dùng(Biết rằng oxi lấy dư 10%)
a)
\(n_{CO_2}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
PTHH: C + O2 --to--> CO2
0,75<-0,75<-----0,75
=> Độ tinh khiết = \(\%C=\dfrac{0,75.12}{10}.100\%=90\%\)
b)
\(n_{SO_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\)
PTHH: S + O2 --to--> SO2
0,025<-0,025<---0,025
=> \(V_{O_2\left(PTHH\right)}=\left(0,025+0,75\right).22,4=17,36\left(l\right)\)
=> \(V_{O_2\left(tt\right)}=\dfrac{17,36.110}{100}=19,096\left(l\right)\)
Đúng 2
Bình luận (0)
B1: tính khối lượng đá vôi (chứa 10% tạp chất ) cần lấy để điều chế 50,4 kg CaO. Hiệu suất phản ứng đạt 90%B2: cho 11,2 lít (đktc) hỗn hợp X gồm CH4 và H2 có tỉ khối so với H2 bằng 3,8 a) tí % thể tích của khí trong X B) Tính Vkk cần dùng để đốt cháy hết hh X trên, giả sử oxi chiếm 20% thể tích kklàm ơn ai giúp mình với, 1 câu thôi cũng được ạmình cần gấp lắm
Đọc tiếp
B1: tính khối lượng đá vôi (chứa 10% tạp chất ) cần lấy để điều chế 50,4 kg CaO. Hiệu suất phản ứng đạt 90%
B2: cho 11,2 lít (đktc) hỗn hợp X gồm CH4 và H2 có tỉ khối so với H2 bằng 3,8
a) tí % thể tích của khí trong X
B) Tính Vkk cần dùng để đốt cháy hết hh X trên, giả sử oxi chiếm 20% thể tích kk
làm ơn ai giúp mình với, 1 câu thôi cũng được ạ
mình cần gấp lắm
Câu 1:
\(m_{CaO(\text {phản ứng})}=\dfrac{50,4}{90\%}=56(g)\\ \Rightarrow n_{CaO}=\dfrac{56}{56}=1(mol)\\ PTHH:CaCO_3\xrightarrow{t^o}CaO+CO_2\\ \Rightarrow n_{CaCO_3}=1(mol)\\ \Rightarrow m_{CaCO_3}=100.1=100(g)\\ \Rightarrow m_{\text {đá vôi}}=\dfrac{100}{90\%}\approx 111,11(g)\)
Đúng 3
Bình luận (0)
BÀI 1: đốt cháy hoàn toàn 14 kg than đá có chứa 96%C, 2,56%S còn lại là tạp chất không cháy. Tính thể tích CO2 và SO2 tạo thành?
BÀI 2: tính thể tích khí oxi cần thiết để đốt cháy hoàn toàn khí Etan (C4H8) có trong 1,8m3 khí chứa 2% tạp chất không cháy. Các thể tích đo được ở điều kiện tiêu chuẩn?
B1:
\(n_C=\dfrac{96\%.14.1000}{12}=1120\left(mol\right)\\ n_S=\dfrac{2,56\%.14.1000}{32}=11,2\left(mol\right)\\ C+O_2\rightarrow\left(t^o\right)CO_2\\ S+O_2\rightarrow\left(t^o\right)SO_2\\ n_{SO_2}=n_S=11,2\left(mol\right)\\ n_{CO_2}=n_C=1120\left(mol\right)\\ V_{CO_2\left(đktc\right)}=1120.22,4=25088\left(l\right)\\ n_{SO_2\left(đktc\right)}=11,2.22,4=250,88\left(l\right)\)
Đúng 1
Bình luận (0)
B2:
\(n_{C_2H_6}=\dfrac{1,8.\left(100\%-2\%\right).1000}{22,4}=78,75\left(mol\right)\\ C_2H_6+\dfrac{7}{2}O_2\rightarrow\left(t^o\right)2CO_2+3H_2O\\ n_{O_2\left(đktc\right)}=\dfrac{7}{2}.78,75=275,625\left(mol\right)\\ V_{O_2\left(đktc\right)}=275,625.22,4=6174\left(l\right)=6,174\left(m^3\right)\)
Đúng 1
Bình luận (0)





























